Рассчитайте титр, титр по хлориду бария
Для реакций осаждения используют раствор, в 50 см3 которого содержится 2,8400 г серной кислоты. Рассчитайте титр, титр по хлориду бария, массовую долю, молярную концентрацию эквивалента и моляльность раствора, если плотность его равна 1,035 г/см3.
Решение: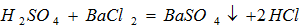
Титр раствора рассчитываем по формуле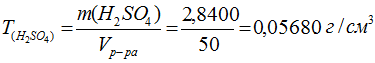
Расчет массовой доли проводим, используя формулу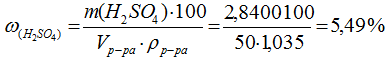
Титр раствора по хлориду бария, это масса его, реагирующая той массой серной кислоты, которая содержится в 1 см3 раствора. Согласно закону эквивалентов: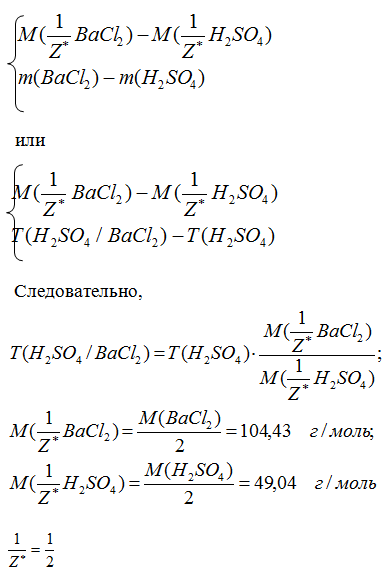
для BaCl2 и H2SO4, так как соль содержит двухзарядный ион Ва2+, а кислота в данной реакции – двухосновная,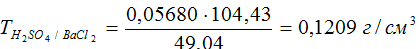
Молярную концентрацию рассчитываем по формуле
М(H2SO4) = 98,08 г/моль
(1000 – коэффициент перевода см3 в дм3)
Молярную концентрацию эквивалента рассчитываем по формулам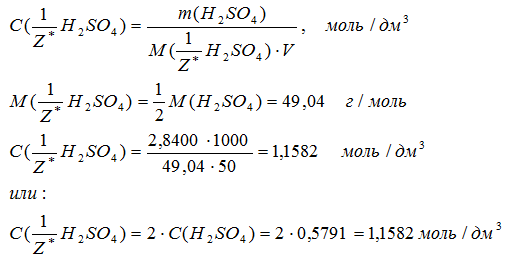
5. Моляльность раствора – количество серной кислоты в 1 кг растворителя. Массу растворителя можно рассчитать как разницу между массой раствора и растворенного вещества: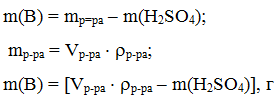
Так как масса серной кислоты в условии задачи дана в г, а плотность в г/см3, то для перевода массы растворителя из г в кг необходимо полученное выражение разделить на 1000. Окончательная формула расчета: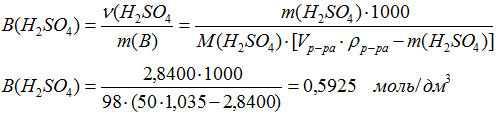
Решать задачу можно, используя формулы, связывающие между собой все способы выражения состава, например: