Определите истинную формулу углеводорода, при сжигании 2,1 г которого получили 6,6 г диоксида углерода и 2,7 г воды
Условие:
Определите истинную формулу углеводорода, при сжигании 2,1 г которого получили 6,6 г диоксида углерода и 2,7 г воды; относительная плотность его паров по воздуху равна 2,90.
Решение
Предполагаемая формула вещества: СaНb. Определение нижних индексов а и b:
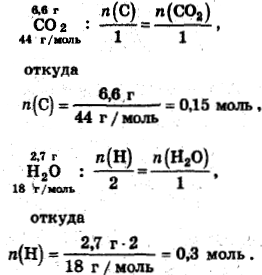
Определение нижних индексов: а: b =n(С): n(Н) =0,15:0.3=1:2,
следовательно, эмпирическая формула: СН2
Расчет молярной массы по относительной плотности:
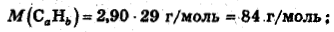
по эмпирической формуле:
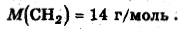
Отношение молярных масс СaНb и CH2:
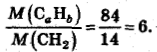
Истинная формула: 2· СН2=С6Н12

