Газ массой 1,236 г при температуре 20 С и давлении 1 атм занимает объем
Условие:
Газ массой 1,236 г при температуре 20 °С и давлении 1 атм занимает объем 512 см3. Вычислите относительную молекулярную массу газа.
Решение Подстановкой в уравнение Клайперона-Менделеева выражения для числа молей v = m/M (где m-масса вещества в граммах, М - его молярная масса) получаем уравнение
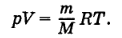
Уравнение Клайперона-Менделеева позволяет, при известных массе и объеме газа,при определенных температуре и давлении, вычислить егомолярную массу М. Поскольку М =Mr г/моль-1, полученный результат соответствует относительной молекулярной массе Мr. Подставляя все данные в условии задачи значения величин в системе СИ, находим
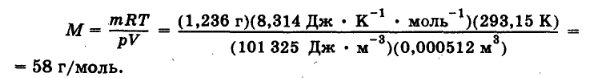
Ответ: Mr = 58 г/моль
категории:

